Šta jerijetka zemlja?
Ljudska bića imaju historiju dugu preko 200 godina, od otkrića rijetkih zemalja 1794. godine. Budući da je u to vrijeme pronađeno malo rijetkih zemalja, hemijskim postupkom mogla se dobiti samo mala količina oksida nerastvorljivih u vodi. Historijski gledano, takvi oksidi su se obično nazivali "zemlja", otuda i naziv rijetka zemlja.
U stvari, rijetki zemni minerali nisu rijetki u prirodi. Rijetki zemni elementi nisu zemlja, već tipičan metalni element. Njihov aktivni tip je odmah iza alkalnih i zemnoalkalnih metala. Imaju veći sadržaj u kori od običnog bakra, cinka, kalaja, kobalta i nikla.
Trenutno se rijetke zemlje široko koriste u raznim oblastima kao što su elektronika, petrohemija, metalurgija itd. Gotovo svakih 3-5 godina naučnici uspijevaju otkriti nove načine korištenja rijetkih zemalja, a od svakih šest izuma, jedan ne može bez rijetkih zemalja.
Kina je bogata rijetkim zemnim mineralima, zauzimajući prvo mjesto na tri svjetske rang-liste: rezerve, obim proizvodnje i obim izvoza. Istovremeno, Kina je i jedina zemlja koja može obezbijediti svih 17 rijetkih zemnih metala, posebno srednje i teške rijetke zemne metale sa izuzetno istaknutom vojnom primjenom.
Sastav rijetkih zemnih elemenata
Rijetkozemni elementi su sastavljeni od lantanoidnih elemenata u periodnom sistemu hemijskih elemenata:lantan(La),cerijum(Ce),prazeodimijum(Pr),neodimijum(Nd), prometij (Pm),samarij(Sm),europijum(EU),gadolinijum(Bog),terbijum(Tb),disprozij(Dy),holmijum(Ho),erbijum(Hm),tulijum(Tm),iterbijum(Yb),lutecij(Lu), i dva elementa blisko povezana s lantanidom:skandij(Naučna oblast) iitrijum(D).

Zove seRijetka zemlja, skraćeno kao Rijetka Zemlja.

Klasifikacija rijetkih zemnih elemenata
Klasificirani prema fizičkim i hemijskim svojstvima elemenata:
Laki rijetki zemni elementi:skandij, itrijum, lantan, cerij, prazeodim, neodim, prometijum, samarijum, europijum
Teški rijetki zemni elementi:gadolinij, terbijum, disprozijum, holmijum, erbijum, tulij, iterbijum, lutecijum
Klasificirano po karakteristikama minerala:
Cerijumova grupa:lantan, cerijum, prazeodimijum, neodimijum, prometijum, samarij, evropijum
Itrijumova grupa:gadolinij, terbijum, disprozijum, holmijum, erbijum, tulij, iterbijum, lutecijum, skandij, itrijum
Klasifikacija ekstrakcijskom separacijom:
Lagane rijetke zemlje (ekstrakcija P204 slabe kiselosti)lantan, cerijum, prazeodimijum, neodimijum
Srednje rijetke zemlje (ekstrakcija P204 niske kiselosti):samarij, europijum, gadolinij, terbijum, disprozij
Teški rijetki zemni metali (ekstrakcija kiselosti u P204):holmijum, erbijum, tulij, iterbijum, lutecijum, itrijum
Svojstva rijetkih zemnih elemenata
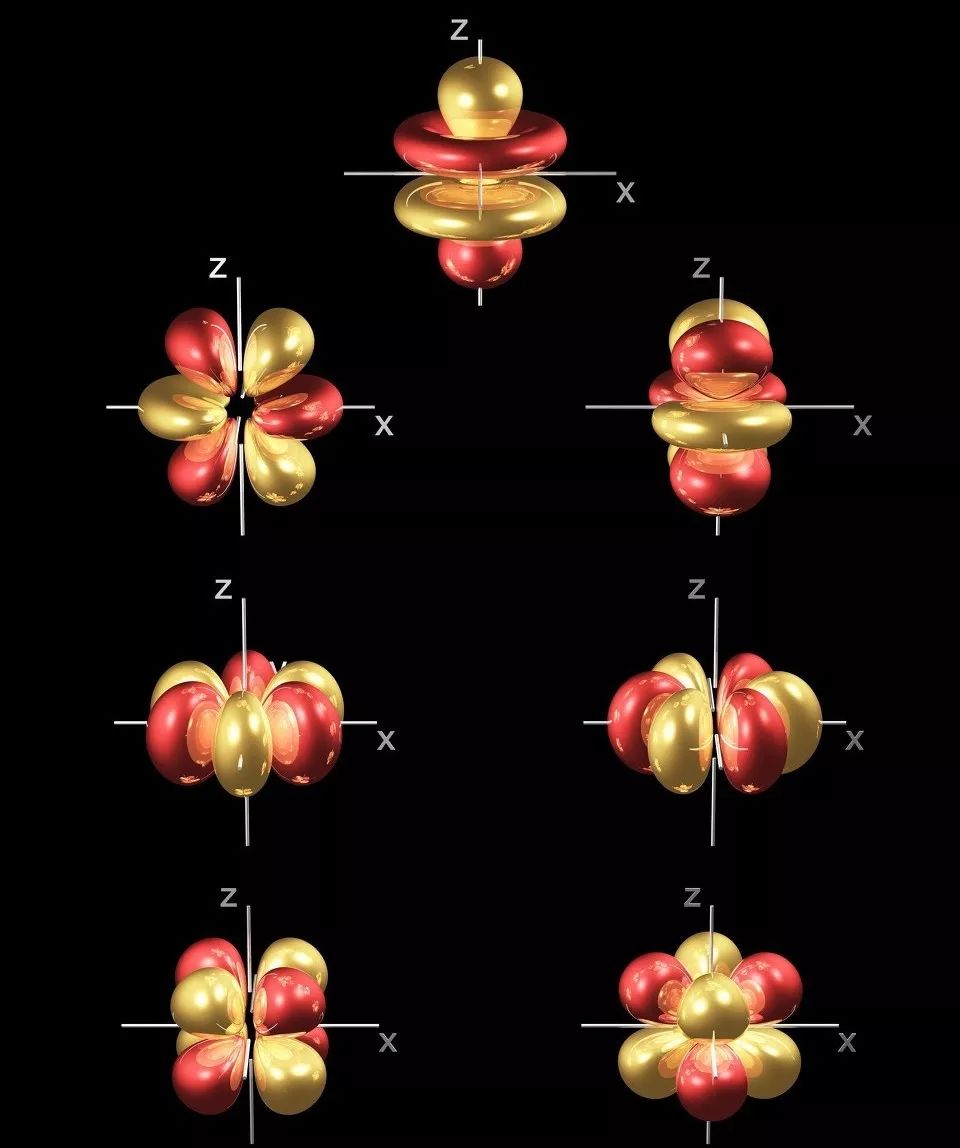
Više od 50 funkcija rijetkih zemnih elemenata povezano je s njihovom jedinstvenom 4f elektronskom strukturom, što ih čini široko korištenim i u tradicionalnim materijalima i u područjima visokotehnoloških novih materijala.
1. Fizička i hemijska svojstva
★ Ima očigledna metalna svojstva; Srebrno je sive boje, osim prazeodimijuma i neodimijuma, izgleda svijetložuto
★ Bogate oksidne boje
★ Formiraju stabilna jedinjenja sa nemetalima
★ Živahni metal
★ Lako oksidira na zraku
2 Optoelektronska svojstva
★ Nepopunjeni 4f podsloj, gdje su 4f elektroni zaštićeni vanjskim elektronima, što rezultira različitim spektralnim članovima i energetskim nivoima
Kada 4f elektroni prelaze u drugu fazu, oni mogu apsorbirati ili emitirati zračenje različitih valnih duljina od ultraljubičastog, vidljivog do infracrvenog područja, što ih čini pogodnim kao luminiscentni materijali.
★ Dobra provodljivost, sposobna za pripremu rijetkih zemnih metala metodom elektrolize
Uloga 4f elektrona rijetkih zemnih elemenata u novim materijalima
1. Materijali koji koriste 4f elektronske karakteristike
★ 4f raspored spina elektrona:manifestuje se kao jak magnetizam – pogodan za upotrebu kao materijali za permanentne magnete, materijali za MRI snimanje, magnetni senzori, supravodiči itd.
★ 4f orbitalni elektronski prijelaz: manifestuje se kao luminiscentna svojstva – pogodno za upotrebu kao luminiscentni materijali kao što su fosfori, infracrveni laseri, vlaknasta pojačala itd.
Elektronski prijelazi u vodećem pojasu energetskog nivoa 4f: manifestiraju se kao svojstva bojenja – pogodni za bojenje i obezbojenje komponenti vrućih tačaka, pigmenata, keramičkih ulja, stakla itd.
2 je indirektno povezan sa 4f elektronom, koristeći jonski radijus, naboj i hemijska svojstva
★ Nuklearne karakteristike:
Mali poprečni presjek apsorpcije termalnih neutrona – pogodan za upotrebu kao strukturni materijali nuklearnih reaktora itd.
Veliki poprečni presjek apsorpcije neutrona – pogodan za zaštitne materijale nuklearnih reaktora itd.
★ Radijus, naboj, fizička i hemijska svojstva rijetkih zemnih jonskih elemenata:
Defekti rešetke, sličan jonski radijus, hemijska svojstva, različita naelektrisanja – pogodno za grijanje, katalizator, senzorski element itd.
Strukturna specifičnost – pogodna za upotrebu kao katodni materijali legura za skladištenje vodonika, materijali za apsorpciju mikrotalasa itd.
Elektrooptička i dielektrična svojstva – pogodna za upotrebu kao materijali za modulaciju svjetlosti, prozirna keramika itd.
Vrijeme objave: 06.07.2023.