Skandij, sa simbolom elementa Sc i atomskim brojem 21, lako je rastvorljiv u vodi, može reagovati sa vrućom vodom i lako potamnjuje na vazduhu. Njegova glavna valencija je +3. Često se meša sa gadolinijem, erbijem i drugim elementima, sa niskim prinosom i sadržajem od približno 0,0005% u kori. Skandijum se često koristi za izradu specijalnog stakla i laganih legura otpornih na visoke temperature.
Trenutno, dokazane rezerve skandija u svijetu iznose samo 2 miliona tona, od čega se 90~95% nalazi u rudama boksita, fosforita i željeza i titana, a mali dio u rudama urana, torija, volframa i rijetkih zemalja, uglavnom raspoređenih u Rusiji, Kini, Tadžikistanu, Madagaskaru, Norveškoj i drugim zemljama. Kina je vrlo bogata resursima skandija, s ogromnim mineralnim rezervama vezanim za skandij. Prema nepotpunim statistikama, rezerve skandija u Kini iznose oko 600.000 tona, koje se nalaze u ležištima boksita i fosforita, ležištima volframa iz porfirnih i kvarcnih žila u Južnoj Kini, ležištima rijetkih zemalja u Južnoj Kini, ležištu rijetke zemlje željezne rude Bayan Obo u Unutrašnjoj Mongoliji i ležištu vanadijum titan magnetita Panzhihua u Sečuanu.
Zbog rijetkosti skandija, cijena skandija je također vrlo visoka, a na svom vrhuncu cijena skandija je bila napuhana 10 puta u odnosu na cijenu zlata. Iako je cijena skandija pala, ona je i dalje četiri puta veća od cijene zlata!
Otkrivanje historije
Godine 1869. Mendeljejev je primijetio razliku u atomskoj masi između kalcija (40) i titana (48) i predvidio da ovdje postoji i neotkriveni element sa srednjom atomskom masom. Predvidio je da je njegov oksid X ₂ O Å. Skandij je 1879. godine otkrio Lars Frederik Nilson sa Univerziteta Uppsala u Švedskoj. Izvadio ga je iz rudnika crnog rijetkog zlata, složene rude koja sadrži 8 vrsta metalnih oksida. Izvadio jeErbijum(III) oksidod crne rijetke zlatne rude i dobijeneIterbijum(III) oksidiz ovog oksida, a postoji i drugi oksid lakšeg elementa, čiji spektar pokazuje da je to nepoznati metal. Ovo je metal koji je predvidio Mendelejev, čiji je oksidSc₂O₃Sam metal skandij je proizveden izSkandijum hloridelektrolitičkim topljenjem 1937. godine.
Mendeljejev
Elektronska konfiguracija
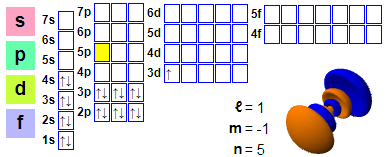
Elektronska konfiguracija: 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Skandijum je mekani, srebrno-bijeli prelazni metal sa tačkom topljenja od 1541 ℃ i tačkom ključanja od 2831 ℃.
Tokom značajnog perioda nakon njegovog otkrića, upotreba skandija nije bila demonstrirana zbog njegove teškoće u proizvodnji. Sa sve većim poboljšanjem metoda odvajanja rijetkozemnih elemenata, sada postoji zreo procesni tok za prečišćavanje skandij spojeva. Budući da je skandij manje alkalan od itrijuma i lantanoida, hidroksid je najslabiji, tako da će se miješani mineral rijetkozemnog elementa koji sadrži skandij odvojiti od rijetkozemnog elementa metodom "stepenog taloženja" kada se skandij(III) hidroksid tretira amonijakom nakon što se prenese u rastvor. Druga metoda je odvajanje skandij nitrata polarnom razgradnjom nitrata. Budući da se skandij nitrat najlakše razgrađuje, skandij se može odvojiti. Pored toga, sveobuhvatno izdvajanje pratećeg skandija iz naslaga urana, torija, volframa, kalaja i drugih minerala također je važan izvor skandija.
Nakon dobijanja čistog skandij spoja, on se pretvara u ScCl Å i topi zajedno s KCl i LiCl. Rastopljeni cink se koristi kao katoda za elektrolizu, što uzrokuje taloženje skandija na cinkovoj elektrodi. Zatim se cink isparava da bi se dobio metalni skandij. Ovo je lagani srebrno-bijeli metal s vrlo aktivnim hemijskim svojstvima, koji može reagirati s vrućom vodom stvarajući vodikov plin. Dakle, metalni skandij koji vidite na slici je zatvoren u boci i zaštićen argonom, inače će skandij brzo formirati tamnožuti ili sivi oksidni sloj, gubeći svoj sjajni metalni sjaj.
Aplikacije
Industrija rasvjete
Upotreba skandija koncentrisana je u vrlo svijetlim smjerovima, i nije pretjerano nazvati ga Sinom svjetlosti. Prvo magično oružje skandija zove se skandijum natrijumova lampa, koja se može koristiti za osvjetljavanje hiljada domaćinstava. Ovo je metal-halogenidna električna lampa: sijalica je napunjena natrijum jodidom i skandijum trijodidom, a istovremeno se dodaju skandijum i natrijumova folija. Tokom visokonaponskog pražnjenja, skandijumovi ioni ioni natrijuma emituju svjetlost svojih karakterističnih talasnih dužina emisije. Spektralne linije natrijuma su 589,0 i 589,6 nm, dvije poznate žute svjetlosti, dok su spektralne linije skandija 361,3~424,7 nm, niz emisija bliske ultraljubičaste i plave svjetlosti. Budući da se međusobno dopunjuju, ukupna proizvedena boja svjetlosti je bijela svjetlost. Upravo zato što skandij-natrijumske lampe imaju karakteristike visoke svjetlosne efikasnosti, dobre boje svjetlosti, uštede energije, dugog vijeka trajanja i snažne sposobnosti razbijanja magle, mogu se široko koristiti za televizijske kamere, trgove, sportske objekte i rasvjetu puteva, te su poznate kao izvori svjetlosti treće generacije. U Kini se ova vrsta lampe postepeno promovira kao nova tehnologija, dok se u nekim razvijenim zemljama ova vrsta lampe široko koristila već početkom 1980-ih.
Drugo magično oružje skandija su solarne fotonaponske ćelije, koje mogu sakupljati svjetlost raspršenu na tlu i pretvarati je u električnu energiju za pokretanje ljudskog društva. Skandij je najbolji metalni barijera u metalnim izolatorima, poluprovodničkim silicijumskim solarnim ćelijama i solarnim ćelijama.
Njegovo treće magično oružje naziva se izvor γ A zraka. Ovo magično oružje može jarko sijati samo po sebi, ali ovu vrstu svjetlosti ne možemo primiti golim okom, već je to protok fotona visoke energije. Obično izdvajamo 45Sc iz minerala, što je jedini prirodni izotop skandija. Svako jezgro 45Sc sadrži 21 proton i 24 neutrona. 46Sc, umjetni radioaktivni izotop, može se koristiti kao izvor γ zračenja ili kao trasirajući atomi koji se također mogu koristiti za radioterapiju malignih tumora. Postoje i primjene poput itrijum-galijum-skandijum-granatnog lasera.Skandijum fluoridStakleno infracrveno optičko vlakno i katodna cijev obložena skandijem na televiziji. Čini se da se skandij rađa sa sjajem.
Industrija legura
Skandijum u svom elementarnom obliku se široko koristi za dopiranje aluminijumskih legura. Čim se aluminijumu doda nekoliko hiljaditih dijelova skandija, formiraće se nova faza Al3Sc, koja će igrati ulogu metamorfoze u aluminijumskoj leguri i značajno promijeniti strukturu i svojstva legure. Dodavanje 0,2%~0,4% Sc (što je zaista slično udjelu dodavanja soli prženom povrću kod kuće, potrebno je samo malo) može povećati temperaturu rekristalizacije legure za 150-200 ℃ i značajno poboljšati čvrstoću na visokim temperaturama, strukturnu stabilnost, performanse zavarivanja i otpornost na koroziju. Također može izbjeći fenomen krhkosti koji se lako javlja tokom dugotrajnog rada na visokim temperaturama. Aluminijumske legure visoke čvrstoće i visoke žilavosti, nove zavarive aluminijumske legure visoke čvrstoće otporne na koroziju, nove aluminijumske legure visoke temperature, aluminijumske legure visoke čvrstoće otporne na neutronsko zračenje itd. imaju vrlo atraktivne izglede za razvoj u vazduhoplovstvu, avijaciji, brodovima, nuklearnim reaktorima, lakim vozilima i brzim vozovima.
Skandijum je također odličan modifikator za željezo, a mala količina skandija može značajno poboljšati čvrstoću i tvrdoću lijevanog željeza. Osim toga, skandijum se može koristiti i kao aditiv za visokotemperaturne legure volframa i kroma. Naravno, osim što se koristi za izradu vjenčanica za druge, skandijum ima visoku tačku topljenja i gustoću sličnu aluminijumu, a koristi se i u lakim legurama visoke tačke topljenja kao što su legura titana od skandija i legura magnezijuma od skandija. Međutim, zbog visoke cijene, uglavnom se koristi samo u visokokvalitetnim proizvodnim industrijama kao što su svemirski brodovi i rakete.
Keramički materijal
Skandijum, pojedinačna supstanca, se uglavnom koristi u legurama, a njegovi oksidi igraju važnu ulogu u keramičkim materijalima na sličan način. Tetragonalni cirkonijev keramički materijal, koji se može koristiti kao elektrodni materijal za gorivne ćelije na čvrsti oksid, ima jedinstveno svojstvo gdje se provodljivost ovog elektrolita povećava s porastom temperature i koncentracije kisika u okolini. Međutim, kristalna struktura ovog keramičkog materijala sama po sebi ne može stabilno postojati i nema industrijsku vrijednost; potrebno je dopiranje nekim supstancama koje mogu fiksirati ovu strukturu kako bi se održala njena prvobitna svojstva. Dodavanje 6~10% skandijevog oksida je poput betonske strukture, tako da se cirkonijev oksid može stabilizirati na kvadratnoj rešetki.
Postoje i inženjerski keramički materijali poput silicijum nitrida visoke čvrstoće i otpornosti na visoke temperature, kao zgušnjivači i stabilizatori.
Kao zgušnjivač,Skandijum oksidMože formirati vatrostalnu fazu Sc2Si2O7 na rubu finih čestica, čime se smanjuje deformacija inženjerske keramike na visokim temperaturama. U poređenju s drugim oksidima, može bolje poboljšati mehanička svojstva silicijum nitrida na visokim temperaturama.
Katalitička hemija
U hemijskom inženjerstvu, skandij se često koristi kao katalizator, dok se Sc2O3 može koristiti za dehidraciju i deoksidaciju etanola ili izopropanola, razgradnju sirćetne kiseline i proizvodnju etilena iz CO i H2. Pt-Al katalizator koji sadrži Sc2O3 također je važan katalizator za procese hidrogenacije i rafiniranja teških ulja u petrohemijskoj industriji. U reakcijama katalitičkog krekiranja kao što je kumen, aktivnost Sc-Y zeolitnog katalizatora je 1000 puta veća od aktivnosti aluminijum silikatnog katalizatora; u poređenju s nekim tradicionalnim katalizatorima, izgledi za razvoj skandij katalizatora bit će vrlo svijetli.
Industrija nuklearne energije
Dodavanje male količine Sc2O3 u UO2 u visokotemperaturnom nuklearnom gorivu reaktora može izbjeći transformaciju rešetke, povećanje volumena i pucanje uzrokovano konverzijom UO2 u U3O8.
Gorivna ćelija
Slično tome, dodavanje 2,5% do 25% skandija u nikl-alkalne baterije povećat će njihov vijek trajanja.
Poljoprivredni uzgoj
U poljoprivredi, sjeme poput kukuruza, repe, graška, pšenice i suncokreta može se tretirati skandij sulfatom (koncentracija je uglavnom 10-3~10-8mol/L, različite biljke će imati različite vrijednosti), a stvarni efekat podsticanja klijanja je postignut. Nakon 8 sati, suha težina korijena i pupoljaka se povećala za 37% odnosno 78% u poređenju sa sadnicama, ali mehanizam se još uvijek proučava.
Od Nielsenove pažnje posvećene dugu podataka o atomskoj masi do danas, skandij je ušao u vidokrug ljudi tek stotinu ili dvadeset godina, ali je gotovo stotinu godina sjedio na klupi. Tek snažan razvoj nauke o materijalima krajem prošlog stoljeća donio mu je vitalnost. Danas su rijetkozemni elementi, uključujući skandij, postali vruće zvijezde u nauci o materijalima, igrajući stalno promjenjive uloge u hiljadama sistema, donoseći više pogodnosti u naše živote svaki dan i stvarajući ekonomsku vrijednost koju je još teže izmjeriti.
Vrijeme objave: 29. juni 2023.