Cerijum je neosporni "veliki brat" u velikoj porodici rijetkih zemalja. Prvo, ukupna količina rijetkih zemalja u kori je 238 ppm, s cerijem sa 68 ppm, što čini 28% ukupnog sastava rijetkih zemalja i zauzima prvo mjesto; Drugo, cerij je drugi rijetki zemni element otkriven devet godina nakon otkrića itrijuma (1794.). Njegova primjena je vrlo široka, a "cerij" je nezaustavljiv.
Otkriće elementa cerija

Carl Auer von Welsbach
Cerijum su otkrili i imenovali 1803. godine Nijemac Kloppers, švedski hemičar Jöns Jakob Berzelius i švedski mineralog Wilhelm Hisinger. Naziva se cerij, a njegova ruda se zove cerit, u spomen na Ceres, asteroid otkriven 1801. godine. U stvari, ova vrsta cerijevog silikata je hidratizirana sol koja sadrži 66% do 70% cerija, dok ostatak čine spojevi kalcija, željeza i...itrijum.
Prva upotreba cerija bila je plinski kamin koji je izumio austrijski hemičar Carl Auer von Welsbach. Godine 1885. pokušao je sa mješavinom magnezija, lantana i itrijum oksida, ali su te mješavine emitovale zeleno svjetlo bez uspjeha.
Godine 1891. otkrio je da čisti torijum oksid proizvodi bolju svjetlost, iako je plava, te je pomiješan sa cerijum(IV) oksidom da bi proizveo jarku bijelu svjetlost. Osim toga, cerijum(IV) oksid se također može koristiti kao katalizator za sagorijevanje torijum oksida.
Cerijum metal

★ Cerijum je duktilan i mekan srebrno-bijeli metal sa aktivnim svojstvima. Kada je izložen zraku, oksidira, formirajući sloj oksida koji se ljušti nalik hrđi. Kada se zagrijava, gori i brzo reaguje s vodom. Uzorak metalnog cerijuma veličine centimetra potpuno korodira u roku od otprilike godinu dana. Izbjegavajte kontakt sa zrakom, jakim oksidansima, jakim kiselinama i halogenima.
★ Cerijum se uglavnom nalazi u monazitu i bastnaezitu, kao i u fisijskim produktima uranijuma, torijuma i plutonijuma. Štetan je za okolinu, posebnu pažnju treba posvetiti zagađenju vodenih površina.
★ Cerijum je 26. najzastupljeniji element, sa 68 ppm u Zemljinoj kori, odmah iza bakra (68 ppm). Cerijum je zastupljeniji od običnih metala kao što su olovo (13 ppm) i kalaj (2,1 ppm).
Cerijumova elektronska konfiguracija
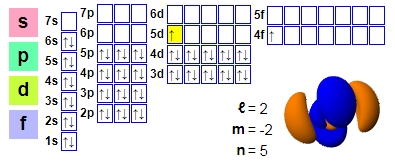
Elektronski aranžmani:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f1 5d1
★ Cerijum se nalazi nakon lantana i ima 4f elektrona koji počinju od cerijuma, što mu olakšava učešće u hemijskim reakcijama. Međutim, 5d orbitala cerijuma je zauzeta, a ovaj efekat nije dovoljno jak u ceriju.
★ Većina lantanoida može koristiti samo tri elektrona kao valentne elektrone, s izuzetkom cerija, koji ima varijabilnu elektronsku strukturu. Energija 4f elektrona je gotovo ista kao i energija vanjskih 5d i 6s elektrona delokaliziranih u metalnom stanju, i potrebna je samo mala količina energije da se promijeni relativna zauzetost ovih elektronskih energetskih nivoa, što rezultira dvostrukom valencijom +3 i +4. Normalno stanje je +3 valencija, što pokazuje +4 valenciju u anaerobnoj vodi.
Primjena cerija

★ Može se koristiti kao aditiv za legure i za proizvodnju cerijevih soli itd.
★ Može se koristiti kao aditiv za staklo za apsorpciju ultraljubičastih i infracrvenih zraka i široko se koristi u automobilskim staklima.
★ Može se koristiti kao odličan materijal za zaštitu okoliša, a trenutno najreprezentativniji je katalizator za prečišćavanje izduvnih gasova automobila, koji efikasno sprječava ispuštanje velike količine izduvnih gasova automobila u zrak.
★ Svjetlorijetki zemni elementiuglavnom se sastoje od cerija kao regulatora rasta biljaka koji mogu poboljšati kvalitet usjeva, povećati prinos i povećati otpornost usjeva na stres.
★ Cerijum sulfid može zamijeniti metale poput olova i kadmija koji su štetni za okoliš i ljude u pigmentima, može obojiti plastiku, a može se koristiti i u industriji premaza i tinte.
★Cerijum(IV) oksidMože se koristiti kao sredstvo za poliranje, na primjer kod hemijsko-mehaničkog poliranja (CMP).
★ Cerij se također može koristiti kao materijal za skladištenje vodika, termoelektrični materijali, cerij-volframove elektrode, keramički kondenzator, piezoelektrična keramika, cerij-silicijum-karbidni abrazivi, sirovine za gorivne ćelije, katalizatori za benzin, trajni magnetski materijali, medicinski materijali, razni legirani čelici i obojeni metali.
Vrijeme objave: 03.07.2023.